子痫前期是严重威胁母胎健康的妊娠期特有疾病。硫酸镁作为子痫前期解痉治疗的一线用药,已广泛应用于临床,但实际应用中仍然有一些困惑,比如诊断重度子痫前期后硫酸镁解痉究竟该用多长时间,轻度子痫前期是否要应用硫酸镁,硫酸镁对胎儿有哪些影响等。另外,由于子痫前期患者血小板激活、微血栓形成,子痫前期与高凝状态相关,抗凝问题也越来越得到重视。发生子痫前期后能否在解痉、镇静和降压等治疗基础上,补加抗凝治疗,抗凝治疗效果如何等尚不明确。现依据我国妊娠期高血压疾病诊治指南(2012版)[1]及世界卫生组织(World Health Organization,WHO)、加拿大、美国、德国、新西兰等相关指南,并结合临床处理经验对子痫前期解痉及抗凝的药物、用药时间等进行阐述。
一、子痫前期的解痉治疗
1.我国指南:我国妊娠期高血压疾病诊治指南(2012版)明确硫酸镁是子痫治疗的一线药物,也是重度子痫前期预防子痫发作的预防用药,对于轻度子痫前期患者也可考虑应用硫酸镁。控制子痫时,硫酸镁静脉负荷剂量为2.5~5 g,溶于10%葡萄糖溶液20 ml静脉推注(15~20 min),或者溶于5%葡萄糖溶液100 ml快速静脉滴注,继而1~2 g/h静脉滴注维持,或者夜间睡眠前停用静脉给药,改为深部肌内注射(25%硫酸镁20 ml+2%利多卡因2 ml臀部肌内注射),24 h总量25~30 g。对于子痫前期或子痫发作后,预防子痫发作时,负荷和维持剂量与子痫发作处理时一致,用药时间长短根据病情需要掌握,一般每天静脉滴注6~12 h,24 h总量不超过25 g。重度子痫前期患者产后应继续使用硫酸镁24~48 h预防产后子痫。用药期间每日评估病情变化,决定是否继续用药。如条件许可,用药期间可定期监测血清镁离子浓度,注意有无镁离子中毒症状[1]。
2.国外相关指南:美国妇产科医师学会(American Congress of Obstetricians and Gynecologists,ACOG)妊娠期高血压疾病诊治指南(2013版)[2]指出,硫酸镁适用于子痫发作、重度子痫前期及子痫前期术中预防子痫发作。负荷剂量4~6 g后,1~2 g/h静脉滴注维持。严重子痫前期患者在分娩前后均应给予硫酸镁。若产后新发高血压合并头痛或视力模糊,或子痫前期孕妇发生重度高血压,建议给予硫酸镁治疗。但对于血压<160/110 mmHg(1 mmHg=0.133 kPa)且无明显症状的孕妇,不建议给予硫酸镁预防子痫发作。
国外相关指南较为统一的观点是,硫酸镁作为子痫发作的一线用药,负荷剂量为4 g,此后维持量为1~2 g/h,并维持至分娩后24 h,或者直至最后一次抽搐后24 h;复发子痫,追加负荷量2~4 g;重度子痫前期患者分娩前后应使用硫酸镁预防子痫发作,并用至分娩后24 h。见表1[3-7]。
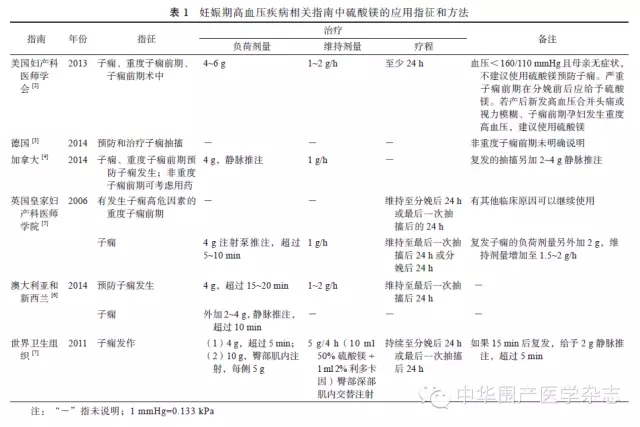
3.我国与国外相关指南的共同点:硫酸镁应用于子痫、重度子痫前期有效,可作为临床子痫发作的一线用药;子痫发作时负荷剂量4~6 g;复发子痫,追加负荷量2~4 g;硫酸镁维持量1~2 g/h;用至最后一次抽搐后的24 h或者分娩后24 h;重度子痫前期应用硫酸镁可以预防子痫发生;重度子痫前期患者分娩前后应及时给予硫酸镁,直至分娩后24 h;产后新发的重度子痫前期也要应用硫酸镁。
4.临床困惑和经验体会:早发型重度子痫前期患者硫酸镁解痉究竟该用多长时间?我国与国外相关指南强调子痫发作时硫酸镁的应用和重度子痫前期患者围分娩期以及分娩后维持治疗。如果重度子痫前期患者,尤其是早发型患者,在控制病情、延长孕周过程中硫酸镁究竟能用多久?其母胎利弊如何权衡?从临床经验来看,产前子痫发生率高于产时和产后子痫,妊娠期更需要预防应用,但长期应用硫酸镁,血镁浓度过高可能会导致母胎毒性作用。2014年美国食品药品监督管理局[8]提出,硫酸镁连续应用超过5~7 d,可能导致婴儿的钙水平降低和骨质改变,包括骨质疏松和骨折,因此建议应用硫酸镁不超过5~7 d。对于轻度子痫前期使用硫酸镁存在一定争议。我国和加拿大妊娠期高血压疾病诊治指南中提及轻度子痫前期可以应用硫酸镁,美国妊娠期高血压疾病诊治指南明确不用,其他指南没有提及。轻度和重度子痫前期均有可能发生子痫。轻度子痫前期患者的子痫发生率约为1/200,重度子痫前期不用硫酸镁治疗时子痫的发生率为1/50,用硫酸镁治疗时子痫发生率明显下降至0.6/100,但对于重度子痫前期本身导致的妊娠期并发症,例如肺水肿、脑卒中、肝脏血肿、肾功能衰竭等,预防效果不明确。我国妊娠期高血压疾病诊治指南(2012版)建议,轻度子痫前期患者应住院进行病情评估[1]。从临床经验来看,可以在住院期间短期应用硫酸镁3~5 d,病情稳定的轻度子痫前期,可停用硫酸镁,但须密切观察病情进展或门诊随访相关指标变化。
二、子痫前期的抗凝治疗
(一)抗凝治疗的益处和风险
我国妊娠期高血压疾病诊治指南(2012版)未对抗凝药物预防子痫前期做出明确规定[1],但国外多数妊娠期高血压疾病诊治指南都肯定了血小板解聚剂阿司匹林预防子痫前期的作用。相关研究表明,小剂量阿司匹林可使子痫前期的发生风险降低2%~5%、早产的发生风险降低2%~4%、胎儿生长受限的发生风险降低1%~5%,且不会增加胎盘早剥、产后出血和胎儿颅内出血等发生风险,不增加围产期病死率[9]。
(二)抗凝药物应用的临床困惑和经验体会
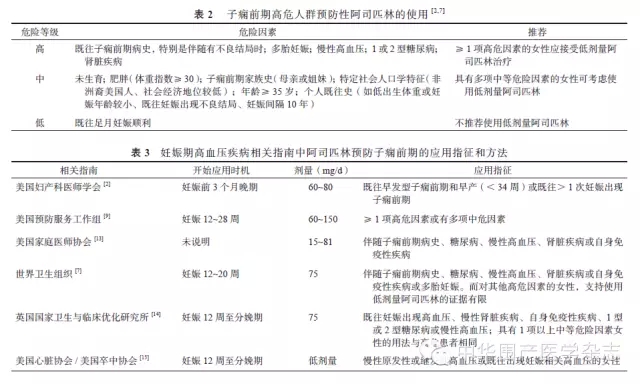
国外妊娠期高血压疾病诊治指南只提及抗凝药物对子痫前期的预防作用[2-7]。见表2。如果高危人群没有在妊娠早、中期给于阿司匹林预防,发生子痫前期后能否在解痉、镇静和降压等治疗基础上补加抗凝治疗?抗凝治疗还有效吗?分析子痫前期的发病机理,胎盘释放纤溶酶原激活抑制剂-1、内皮素等组织因子等增加,导致血管痉挛、血管通透性增加、血浆外漏,出现血容量相对不足,血液浓缩,血液处于高凝状态;可溶性fms-样酪氨酸激酶-1和可溶性内皮因子等多种组织因子导致血管内皮细胞损伤、血小板激活、局部聚集形成微血栓,子痫前期的这些病理改变与高凝状态密切联系,也为抗凝治疗提供了理论依据。动物研究发现,抗凝可以改善子痫前期的高凝状态[10],也许可以用于子痫前期的辅助治疗。
(三)抗凝药物分类及联合应用的疗效和安全性
1.阿司匹林:阿司匹林可以有效抑制血小板的黏附、聚集和释放,防止血栓形成。口服阿司匹林可防止血液高凝状态,多用于预防高危孕妇血栓形成,且妊娠期小剂量使用安全可靠[11-12]。国外各妊娠期高血压疾病诊治指南明确了阿司匹林的使用指征和方法(表3)。我国妊娠期高血压疾病诊治指南(2012版)虽未对阿司匹林抗凝治疗进行详细说明[1],但结合中国人群特点,对于子痫前期高危患者建议给予小剂量阿司匹林治疗,并定期监测血小板计数和血小板聚集功能,及时调整药物剂量。
其他多种常用抗血小板药物,包括潘生丁、磺吡酮、噻氯匹定、芬氟咪唑、氢氯吡格雷等,在妊娠期使用的安全性尚未得到充分证实,临床应用有限。
2.低分子肝素和肝素:低分子肝素是20世纪70年代发展起来的一种新型抗凝药物,与普通肝素相比,低分子肝素与血浆蛋白结合度低,皮下注射生物利用度好(90%),生物半衰期长(2.8~4.1 h),是普通肝素(1 h)的2~4倍,抗凝效果呈明显的量效关系,每日仅需给药1~2次,抗血栓作用增强2~4倍,出血等不良反应少,并可通过监测凝血因子和血小板计数判断治疗效果和安全性。低分子肝素无胎儿毒性及致畸性,美国食品药品监督管理局定为B类药物,药物不通过胎盘,不分泌于乳汁,妊娠期及分娩期使用均安全,国外多个妊娠期高血压疾病诊治指南已将低分子肝素列为首选药物[4,6]。小剂量低分子肝素(1支/d)可用于预防,大剂量低分子肝素(1支/12 h)用于治疗。但抗凝治疗仍存在一定风险,如鼻出血、血尿、消化道出血、颅内出血、产科出血、血小板降低等。建议定期监测出凝血指标和血常规,尤其关注临床出血症状和血小板计数的变化。
3.抗凝药物联合应用的疗效和安全性:阿司匹林和低分子肝素的抗凝作用环节不同,前者是使血小板的环氧合酶(即前列腺素合成酶)乙酰化,抑制环内过氧化物的生成,减少血栓素A2的生成,从而抑制血小板聚集,减少血栓形成;后者主要阻断Ⅹ因子的活化,阻止纤维蛋白凝块的形成,如果联合应用,可以增加抗凝疗效。因此,产科严重高凝状态的人群可以联合应用,但必须更加严密地动态监测出凝血状态,比如血小板计数和血小板功能、D-二聚体、纤维蛋白降解产物、凝血因子和肝功能等。
(四)抗凝治疗期间麻醉及围分娩期处理
关于对非妊娠期患者放置硬膜外导管后接受肝素治疗导致硬膜下血肿的相关文献报道逐渐增多,因此不建议接受抗凝治疗的患者使用局部区域性阻滞麻醉。应用抗凝药物的孕妇行计划性引产和剖宫产时,如果凝血指标调整至规定范围内,仍可考虑使用区域性阻滞麻醉[16-17],伤口渗血问题鲜有发生。如应用低分子肝素后12~24 h,手术前停用阿司匹林7 d以上,可实施椎管内麻醉,拔管后12~24 h再用低分子肝素进行抗凝治疗,发生硬膜外血肿的风险较低,无产后出血发生率增加的报道。如果没有在规定时间内预期停用抗凝药物或者紧急手术,则宜选用全身麻醉。鱼精蛋白拮抗肝素和低分子肝素有效,但有过敏风险,出血严重者才考虑使用。
参考文献(略)
 妇产科在线APP下载
妇产科在线APP下载









 京公网安备 11010202008857号
京公网安备 11010202008857号