子宫内膜异位症(内异症)是一种良性疾病,但其侵袭、播散等生物学行为却和恶性肿瘤类似,可导致周期性痛经、性交痛、不孕等症状,对患者的生活质量产生影响。现有的治疗方法均有一定局限性,尤其是术后5年高达50%的复发率[1],使得“复发”一词犹如达摩克利斯之剑始终悬于每一个内异症患者的头顶。目前广泛提倡的术后长期管理策略经临床实践证明能够降低复发风险,但不可否认的是,长期药物治疗对患者家庭及社会造成了沉重的经济负担,并对患者的依从性提出了挑战。同时长期应用GnRH-a、口服避孕药等激素类药物增加了肝功能损害、骨质丢失、血栓形成等风险。因此,如何更好地控制内异症的术后复发是一项亟待解决的临床需求,也是改善内异症治疗效果的关键。
基于多年医疗经验和科学研究,在刘惜时教授的带领下,复旦大学附属妇产科医院子宫内膜异位性疾病团队围绕内异症的发生机制、病理生理、复发、疼痛机制等课题,从事大量与临床相关的科学研究,开创多个内异症科研先河,在国际相关领域达到领先水平。基于该团队大量的前期研究,该团队开创性地提出,围手术窗口期干预减少内异症术后复发风险的新思路[2]。
近日,该团队在妇产科Q1区期刊《生殖生物医学在线》(RBMO,IF:3.2)发表了术前和围术期干预对内异症术后复发影响的研究结果,发现围手术窗口期药物干预减轻内异症因微小残留病灶或病灶碎片播散种植所导致的术后复发病灶重量、纤维化程度,并缓解小鼠痛觉过敏。提示简单合理的药物干预能够有效抑制内异症的术后复发,有望为内异症的临床治疗带来新的思路和突破。

在这项最新的研究中,探究了围手术窗口期干预对内异症术后复发的作用,基于内异症可能的术后复发机制,该团队构建了小鼠内异症术后复发模型—微小残留复发模型(The incomplete excision (IE) model)、播散复发模型(The spillage and dissemination (S&D) model),于术前运用酮咯酸,围手术窗口期运用普萘洛尔+穿心莲内酯、阿瑞匹坦进行分析。
采用Balb/C 小鼠建立子宫内膜异位症模型后2周,随机分组通过手术构建小鼠内异症术后复发模型:
(1)微小残留复发模型(The IE model)[3]:术中选择性切除内异症病灶,保留完整小病灶模拟术中微小病灶残留(残留病灶数量不超过2枚,直径均小于0.5 mm),以温热生理盐水充分冲洗腹腔。
(2)播散复发模型(The S&D model):术中切除探及的所有内异症病灶,以温热生理盐水充分冲洗腹腔;选取2枚直径约0.5 mm病灶充分剪碎,与生理盐水配至100 ul,将其中50 ul注射于小鼠左下腹腔模拟术中播散的内异症病灶碎片。
在术前2小时及术后24小时给予各组小鼠相应药物灌胃治疗,并在术后3/4周评估复发病灶及小鼠疼痛情况。分析发现,术前及围术期药物干预的小鼠疼痛缓解,复发病灶重量明显减轻,纤维化程度明显降低,病灶组织E-cadhein、PR-B表达显著升高,ADRB2、VEGF、p-p65、α -SMA表达显著降低(图1)。
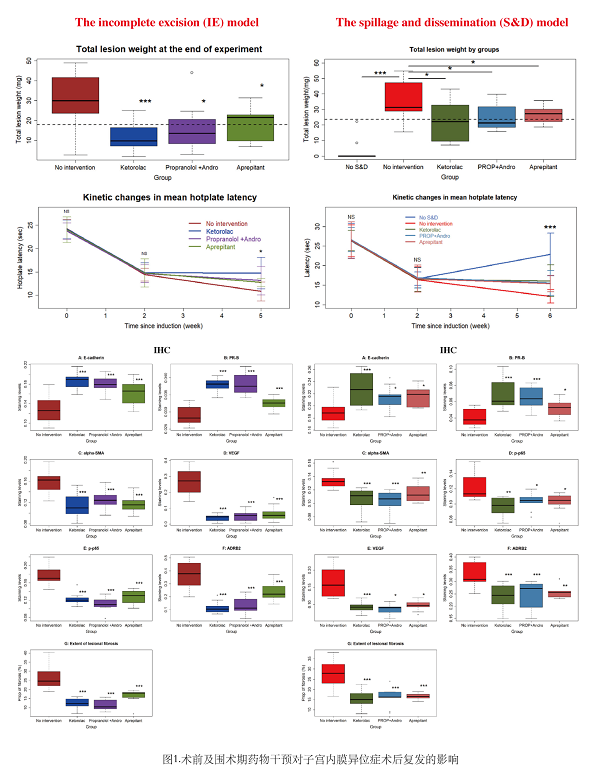
其中病变纤维化程度与E-cadherin、PR-B染色水平呈负相关,与VEGF,p-p65,α-SMA,ADRB2染色水平呈正相关;ADRB2染色水平与内异症复发病灶重量、纤维化程度、a-SMA、p-p65、VEGF染色水平呈正相关。
一、在既往所建立的微小残留复发模型(The IE model)基础上,成功构建术中播散复发模型(The S&D model),为进一步了解内异症的复发机制、探索围手术窗口期干预提供了实验动物模型。
在内异症研究中,啮齿动物模型因其成本低、实验条件易实现及遗传操作可用性,成为重要的基础研究模型。实验中构建的微小残留复发模型(The IE model)和播散复发模型(The S&D model)涵盖了相当一部分在人类中观察到的复发内异症病例,为进一步探索内异症围手术窗口期的干预提供了实用的动物模型。
二、基于既往研究基础--手术应激、炎症反应促进内异症发生发展,创新性地在围手术窗口期运用非激素类药物干预,显著降低了小鼠内异症术后复发风险,为抑制内异症复发提供新思路,为人类临床试验提供科学依据。
刘惜时教授团队前期已证明了手术对内异症发生发展的促进作用[4,5],即手术应激激活下丘脑-垂体-肾上腺素能(HPA)轴和交感-肾上腺髓质(SAM)轴,诱导炎症反应、抑制细胞免疫、促进新生血管形成。基于上述机制,该文中选用了酮咯酸、普萘洛尔+穿心莲内酯、阿瑞匹坦进行分析,结果一致显示,围手术窗口期干预显著减轻了小鼠复发病灶重量、病灶纤维化程度,并改善小鼠疼痛。
三、酮咯酸以其高效的抗炎作用、出色的安全性首次应用于动物复发模型,证明在内异症复发中具有显著抑制作用。
酮咯酸是一种非甾体类抗炎药(NSAID),凭借良好的镇痛作用及出色的安全性在临床中得到广泛应用。在此次研究中,术前运用酮咯酸能够通过抑制COX-1/TXA2信号通路,早期阻断炎症级联反应、促进炎症消退、解除细胞免疫抑制,抑制内异症术后复发。
鉴于内异症术后的高复发率,应用激素类药物的长期管理策略已成为常态。临床实践证明长期管理策略行之有效,但不可否认仍具有药物副作用多、患者经济负担重等缺陷。基于围手术窗口期产生的应激、炎症反应、细胞免疫抑制等一系列生物学改变,我们针对性地选用了非激素类药物方案进行干预,所取得的实验结果鼓舞人心。但仅有动物实验数据支持显然不够,正如RBMO杂志评述所提及,是时候开展进一步的临床研究,通过HPO激素轴以外的途径,探究围手术窗口期干预的有效性及其潜在的作用机制。
八千里路云和月,探索降低内异症术后复发的科研之路仍道阻且长。莫等闲,迎难而上行则将至!希望我们的研究成果能造福更多患者。期待与各位同道精诚合作、携手共进。心之所善,当上下求索。行而不辍,未来可期!

参考文献:
[1] Liu X, Long Q, Guo SW. Surgical History and the Risk of Endometriosis: A Hospital-Based Case-Control Study. Reprod Sci. 2016 Sep;23(9):1217-24.
[2] Guo SW, Martin DC. The perioperative period: a critical yet neglected time window for reducing the recurrence risk of endometriosis? Hum Reprod. 2019 Oct 2;34(10):1858-1865.
[3] Long Q, Zheng H, Liu X, Guo SW. Perioperative Intervention by β-Blockade and NF-κB Suppression Reduces the Recurrence Risk of Endometriosis in Mice Due to Incomplete Excision. Reprod Sci. 2019 May;26(5):697-708.
[4] Long Q, Liu X, Guo SW. Surgery accelerates the development of endometriosis in mice. Am J Obstet Gynecol. 2016 Sep;215(3):320.e1-320.e15.
[5] Long Q, Liu X, Qi Q, Guo SW. Chronic stress accelerates the development of endometriosis in mouse through adrenergic receptor β2. Hum Reprod. 2016 Nov;31(11):2506-2519.
作者介绍

刘惜时教授、郭孙伟教授的研究《子宫内膜异位症中NF-κB/PR-B失平衡机制的研究及其临床转化应用》,获得2014年中华医学科技奖三等奖、上海医学科技奖二等奖。刘惜时教授在2019年美国生殖年会上获“内异症组最佳基础研究奖”。
刘惜时教授、郭孙伟教授申请获得发明专利《一种用于子宫内膜异位症疾病的检测试剂》。
近年来,团队成员共主持国家自然科学基金资助项目11项(其中重点项目1项),主持上海市课题5项。近5年,团队成员以第一作者/通讯作者发表内异症相关论文80篇。其中,影响因子最高的是郭孙伟教授2019年发表在Nature reviews.Endocrinology杂志的评论,影响因子达16.283。
郭孙伟教授在2015年-2021年,连续7年被爱思唯尔(Elsevier)评选为中国医学领域高被引学者。
Expertscape网站分析评价2010-2020年子宫内膜异位症领域专家的研究水平,郭孙伟教授排名全球前0.042%,跻身世界前十五。刘惜时教授排名全球前0.17%。在2020年中国妇产科领域国际学术影响力排名中,郭孙伟教授位居全国第二。
陈旖珊医生,2020年毕业于复旦大学附属妇产科医院,获(四证合一)专业型硕士学位。主要研究方向:围手术窗口期药物干预对子宫内膜异位症术后复发的影响。
撰稿:陈旖珊
审稿:刘惜时
声明:本文由子宫内膜异位性疾病团队供稿,经审核后发布,如需转载,请注明出处。
 妇产科在线APP下载
妇产科在线APP下载













