多年以来,以铂类为基础的化疗在卵巢癌治疗中始终占据着举足轻重的地位。但对于反复复发的后线卵巢癌患者来说,不仅可选的化疗药物变少,化疗效果不佳,而且还会产生耐药现象,给患者的生命带来极大威胁。为此,人们试图使用作用机制完全不同的新型药物替代化疗,“去化疗”的理念随之萌生。
近年来,PARP抑制剂不仅在卵巢癌维持治疗中大放异彩,而且还被认为可在“去化疗”中扮演重要角色。作为PARP抑制剂中的后起之秀,帕米帕利已被获批在中国既往经过二线及以上化疗的伴有胚系BRCA(gBRCA)突变的复发性晚期卵巢癌、输卵管癌或原发性腹膜癌患者的治疗[1]。
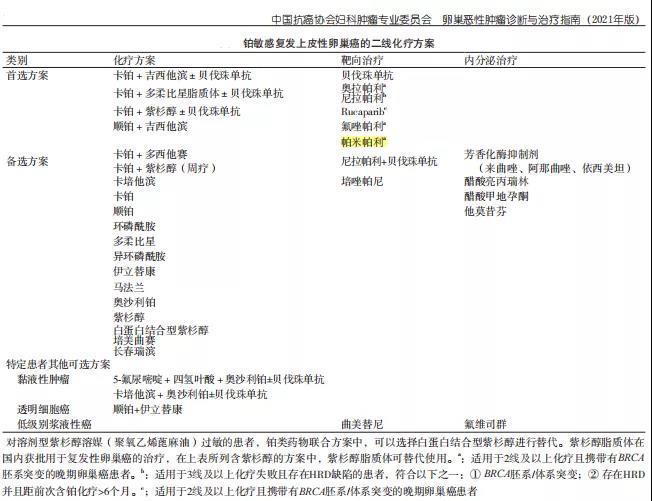
这项批准打破了以往PARP抑制剂仅用于维持治疗的局限,使得患者不用再次承受化疗的痛苦,令卵巢癌的“去化疗”日益走进现实。鉴于此,在中国抗癌协会妇科肿瘤专业委员会编纂的《卵巢恶性肿瘤诊断与治疗指南(2021年版)》中,帕米帕利被列为铂耐药和铂敏感复发上皮性卵巢癌的首选二线治疗方案[2]。

独特药物机制加持,为复发卵巢癌患者带来新生
帕米帕利是一款PARP抑制剂,同时也是百济神州自主研发的第三款抗癌新药。在帕米帕利的研发过程中,得到了国家重大新药创制专项支持,上市许可申请亦被国家药品监督管理局药品审评中心纳入至优先审评队列。此次帕米帕利获得权威指南推荐,意味着该药物的有效性和安全性赢得了医学界的全面认可,卵巢癌患者的治疗也因此更加有的放矢。
PARP抑制剂的抗癌作用主要基于“合成致死”效应[3]。正常情况下,细胞出现DNA单链断裂时,可依赖PARP酶通过碱基切除修复(BER)途径进行修复。当PARP抑制剂作用于肿瘤细胞时,PARP酶无法发挥作用,抑制BER导致复制叉停滞,进而形成DNA双链断裂。
如果肿瘤细胞的BRCA1/2和其他同源重组修复(HRR)通路相关的基因突变或表观遗传学改变,使得DNA损伤后正常修复能力受到抑制,将引起同源重组修复缺陷(HRD),那么在PARP抑制剂作用下不断形成的DNA双链断裂将无法通过HRR途径得到有效修复,两者的“合成致死”效应最终导致肿瘤细胞死亡。
除发挥“合成致死”效应之外,帕米帕利的优异表现还与其独特的药物设计[4]有关。
帕米帕利是目前已知唯一的非P-糖蛋白底物的PARP抑制剂,故而药物摄入体内后,P-糖蛋白无法将其泵出细胞外,因此帕米帕利在肿瘤细胞内的浓度要高于其他的PARP抑制剂,并且始终维持较好的胞内浓度,使药物的耐药性降低,有效性大大增加。
在帕米帕利的化学结构修饰上,研究者特别引入了氮原子以提高药物分子的溶解度,“并环”的化学结构降低了药物的清除率,从而提高了口服药物的生物利用度,而且还能增加帕米帕利穿透血脑屏障的能力。
帕米帕利的高捕获能力也是其重要优势之一,它可选择性地对PARP1和PARP2进行捕获,并且在很低的浓度下就有很高的选择性。
另外,帕米帕利还有血浆蛋白结合率高,通过肾脏和粪便双通道排泄,不损伤肝脏,与其他药物相互作用可能性小等特点,这些都能为患者带来疗效和安全性等多方面的益处。
引领“去化疗”进程,满足卵巢癌治疗未及之需
帕米帕利获准上市主要基于一项1/2期临床试验(NCT03333915)的关键性2期部分的临床结果。该研究提供的有效性和安全性证据为帕米帕利纳入指南推荐提供了坚实的基础。
研究在中国入组了113例既往接受过至少两线标准化疗、携有BRCA1/2突变的高级别上皮性卵巢癌(OC,包括输卵管癌或原发性腹膜癌)或高级别子宫内膜上皮样癌患者。队列1纳入了90例晚期铂敏感OC (PSOC)患者,队列2纳入了23例晚期铂耐药OC(PROC)患者,试验的主要终点为客观缓解率(ORR)。
结果显示,接受帕米帕利治疗的晚期PSOC患者的中位随访时间为17.0个月,ORR为68.3%,中位缓解持续时间(DOR)为13.8个月;晚期PROC患者的中位随访时间为11.6个月,ORR为31.6%,DOR为11.1个月[5][6]。
尤为引人注目的是,无论是PSOC患者还是PROC患者,均可从帕米帕利的治疗中获益[6]。
此前,PSOC经评估后虽可选择手术和/或以铂类为基础的化疗,但随着复发次数增多,PSOC会逐渐转变为PROC。而PROC患者的治疗在临床上更加棘手,目前还没有疗效令人满意的药物,需要频繁更换治疗方案,患者在这一过程中蒙受了相当多的痛苦。可以说,帕米帕利的上市极大缓解了“生命不息,化疗不止”的卵巢癌患者的未及之需。
在安全性方面,帕米帕利同其他PARP抑制剂一样,不良反应(AE)以血液学毒性为主,其他不良反应大多为1~2级。研究显示,口服帕米帕利60 mg BID单药治疗,91.1%的患者可以使用帕米帕利完成既定的治疗计划,坚持长期用药,且持续治疗未终止,仅有7.1%的患者因AE而停药。由此可以看出,帕米帕利的安全性表现良好,有助于临床医生对患者进行管理[6]。
如何在卵巢癌后线治疗中突破传统化疗的局限,帕米帕利正在其中发挥着重要引领作用,并成为复发性卵巢癌“去化疗”的新选择。可以预见,随着帕米帕利被纳入权威指南的推荐,将会为越来越多铂敏感及铂耐药复发患者带来更长的复发间隔、更好的疾病控制和更佳的生存获益。
参考资料:
[1] https://www.nmpa.gov.cn/yaowen/ypjgyw/20210507094042167.html
[2] 中国抗癌协会妇科肿瘤专业委员会. 卵巢恶性肿瘤诊断与治疗指南(2021年版)[J].中国癌症杂志, 2021, 31(6): 474-484.
[3] Xie H, Wang W, Xia B, et al. Therapeutic applications of PARP inhibitors in ovarian cancer[J]. Biomedicine & Pharmacotherapy, 2020, 127: 110204.
[4] Mateo J, Lord C J, Serra V, et al. A decade of clinical development of PARP inhibitors in perspective[J]. Annals of Oncology, 2019, 30(9): 1437-1447.
[5] 百汇泽®胶襄说明书;数据截至时间2020.8.24日
[6] Xiaohua Wu, et al. ESMO poster 820 ;数据截至2020年2月2日
 妇产科在线APP下载
妇产科在线APP下载









 京公网安备 11010202008857号
京公网安备 11010202008857号