卵巢恶性生殖细胞肿瘤(MOGCT)是罕见的卵巢恶性肿瘤,约占所有卵巢恶性肿瘤的5%,但在亚洲人群中占到15%[1]。MOGCT主要发生在青春期和年轻女性中,病灶常位于单侧,大约70%的患者在诊断时为早期。下面为大家阐述这种卵巢恶性肿瘤患者保留生育功能的策略和方法。

一、MOGCT概述
MOGCT具有异质性,根据不同的形态学和分子特征,可分为未成熟畸胎瘤、无性生殖细胞瘤、卵黄囊瘤(又称内胚窦瘤)、原发性绒癌和混合生殖细胞肿瘤。可以说在妇科癌症编年史上,MOGCT在治疗和预后方面有着非凡的进展。在20世纪60年代中期之前,几乎所有患病的年轻女孩和妇女要么死于疾病,要么治愈但却终生不能怀孕。
在随后的50年内,手术和化疗的巨大发展使得罹患这种恶性肿瘤的女性既可以保留生育能力,也可以彻底治愈。据最近的一篇文献报道,无性生殖细胞瘤女性的5年生存率接近100%,非无性生殖细胞瘤女性的5年生存率达85%,其中预后最差的是胚胎癌,5年总生存率仅33.3%[2]。
二、MOGCT患者保留生育功能的可行性与必要性
MOGCT的中位发病年龄据文献统计在19~25岁不等,大多数患者尚未生育,有强烈的保留生育能力的需求。最近一项SEER数据分析结果显示,MOGCT患者中单身女性占该病例队列的近70%。除无性生殖细胞瘤的双侧发病率在10%~15%外,双侧卵巢生殖细胞瘤是极其罕见的,这也为保留生育功能提供了可能性。除此之外,MOGCT对化疗极为敏感,大多数患者预后良好,即使是晚期患者,治愈率也至少可以达到75%[3]。
目前已有多项研究证实MOGCT患者保留生育功能的安全性及有效性。最早的相关研究是由Kurman和Norris在1977年进行的,在182例接受保育手术的早期MOGCT患者队列中,没有观察到预后的差别[4]。随后的一些研究支持这一结果,表明保留生育功能的手术(FSS)不仅在疾病早期,而且在疾病晚期都是可行和安全的。
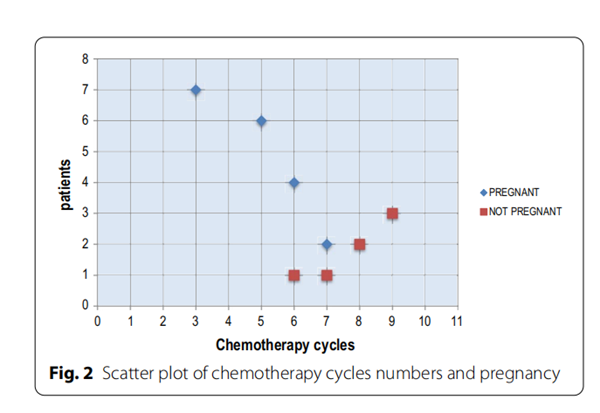
在最近的一项研究中,Zamani等对79例接受保留生育功能治疗的MOGCT患者进行了长达15年的随访。结果显示,患者的5年总生存率达到94.4%,所有未进行辅助化疗的患者月经均正常,辅助化疗组在治疗结束时78%的患者月经恢复正常,妊娠结局与化疗周期数无关。在26例尝试怀孕的患者中有19例成功分娩(73%),没有一例患者需要进行不孕相关治疗。据最新一些文献报道,MOGCT患者治疗后的绝经率在3%~7.4%之间,卵巢早衰率在3.4%~5%之间,以上数据似乎还是比较乐观的[5-6]。
三、MOGCT患者保留生育功能的治疗策略
1、术前评估
对于患有盆腔肿物的年轻患者,尤其是巨大包块,首要要排除恶性肿瘤的可能性。如果考虑有恶性肿瘤的可能性,患者应转诊到妇科肿瘤医生处。这类患者临床管理的关键因素包括术前的评估(体格检查、肿瘤标记物和影像学)以确定恶性肿瘤的可能性、适当的术前咨询(包括对保留生育能力的讨论)、手术入路的选择(随着微创手术实践的增加,微创手术有可能导致医源性肿瘤破裂,使得肿瘤升级,因而切忌不能盲目追求微创手术),除此之外,在许多情况下,即使是最专业的妇科病理学家也不能做出精确的冷冻切片诊断。
在这种情况下,对于年轻女性通常采用较保守的手术范围,需要将术后病理升级后需要追加手术的可能性充分告知患者及其家属。妇科肿瘤医生也必须对肿瘤每个亚型的生物学行为有全面的了解,以便优化后续临床管理的建议,包括监测和生殖咨询,以确定如何在适当的时机最好地结合生育能力保护策略。
2、手术治疗
NCCN指南提出,对于有生育要求者,子宫和对侧附件正常者可行保留生育功能的全面分期手术,术后可用超声随访监测,完成生育后可考虑接受根治性手术(2B类证据)。对无生育要求者则行全面分期手术。欧洲肿瘤内科学会(ESMO)称,对于每一位希望保留其生育潜力的MOGCT女性,即使是患有晚期疾病的女性,也可采用保留生育能力的方法。
目前,行保留子宫和对侧卵巢的保留生育能力的手术,是所有希望保留其生殖力的早期MOGCT患者治疗的“金标准”。卵巢恶性肿瘤患者的全面分期术包括大网膜切除术、腹腔冲洗液留取、腹膜多点活检、子宫切除术、卵巢输卵管切除术(BSO)和淋巴结切除术。
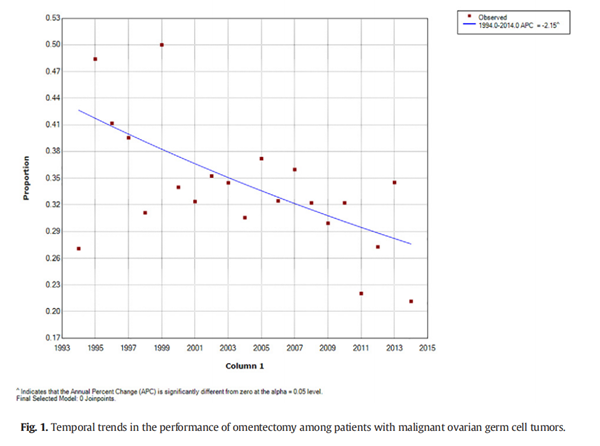
然而,考虑到MOCGT通常对化疗极为敏感,这类患者所需的手术分期范围仍然存在争议。最近的一项研究显示,近20年来MOGCT患者的手术治疗范围发生了很大变化,大网膜切除术、BSO和子宫切除术的比例呈下降趋势,特别是在年轻的患者中,这反映了外科医生的实践变化。Nasioudis等学者在一项研究中共纳入2238例MOCGT患者,中位年龄21岁。在这些患者中只有12.4%接受了子宫切除术,1/3接受了大网膜切除术,一半接受了淋巴结切除术,结果证实并没有明显的生存差异[7]。
淋巴结切除术(LND)旨在识别隐匿性淋巴结转移并指导术后治疗,但同时也延长了手术时间,并且可能导致盆腔粘连。目前已有很多研究证实LND并没有为MOCGT患者带来生存获益。有趣的是,研究也同时证实,是否存在淋巴结转移对患者的生存没有显著影响。
对于大网膜切除术,Xu等分析了223例临床早期MOGCT患者,其中74%接受了大网膜切除术。行大网膜切除术的患者与未行大网膜切除术组的10年生存率相当,差异没有统计学意义(92% vs. 97.9%,P=0.34)[8]。因此,目前普遍认为,在大网膜外观没有明显异常的情况下,可以不常规行大网膜切除术,而由大网膜活检取代。
此外,大量研究证据表明,对侧卵巢切除或活检与生存获益无关,并且可能导致盆腔粘连和卵巢功能衰退,继而引起继发性不孕。2021年FIGO癌症报告也明确提出,不建议对外观正常的卵巢进行活检[9-12]。总而言之,MOGCT患者的手术方式趋向于向更保守的范围转变。
2、辅助治疗
2022年NCCN指南建议,Ⅰ期无性细胞瘤、Ⅰ期G1未成熟畸胎瘤术后可随访。儿童和青春期的ⅠA期和ⅠB期无性细胞瘤、ⅠA期G1未成熟畸胎瘤、ⅠA期胚胎癌和ⅠA期卵黄囊瘤,可选择化疗或观察。任何期别的胚胎癌和卵黄囊瘤、Ⅱ~Ⅳ期无性细胞瘤、Ⅰ期G2~3和Ⅱ~Ⅳ期未成熟畸胎瘤、任何期别的非妊娠性绒癌患者,术后均需化疗[13]。ESMO指南认为,对于IA期无性生殖细胞瘤或IA期1级未成熟畸胎瘤患者,可以省略辅助化疗;对于IA期G2~G3和IB~IC期未成熟畸胎瘤患者,辅助化疗的必要性仍存在争议[14]。
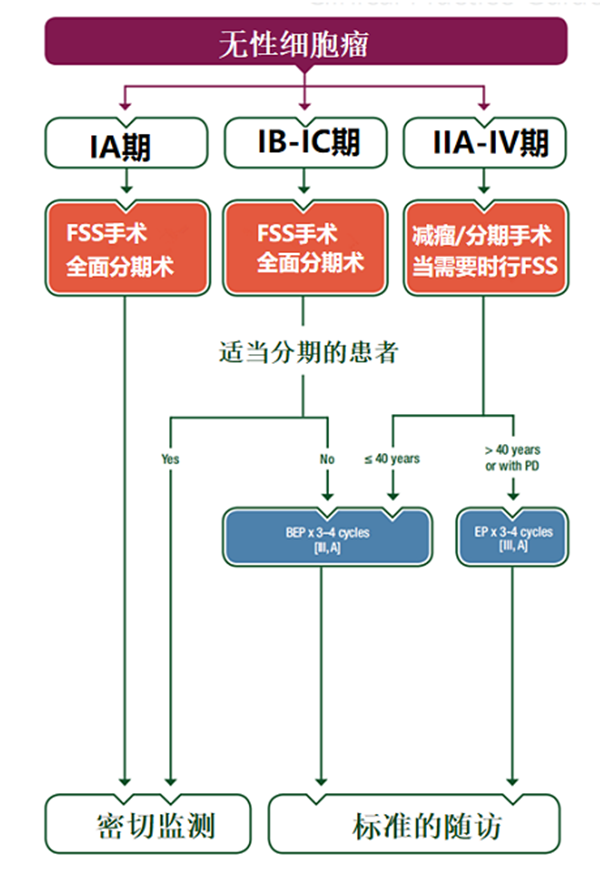
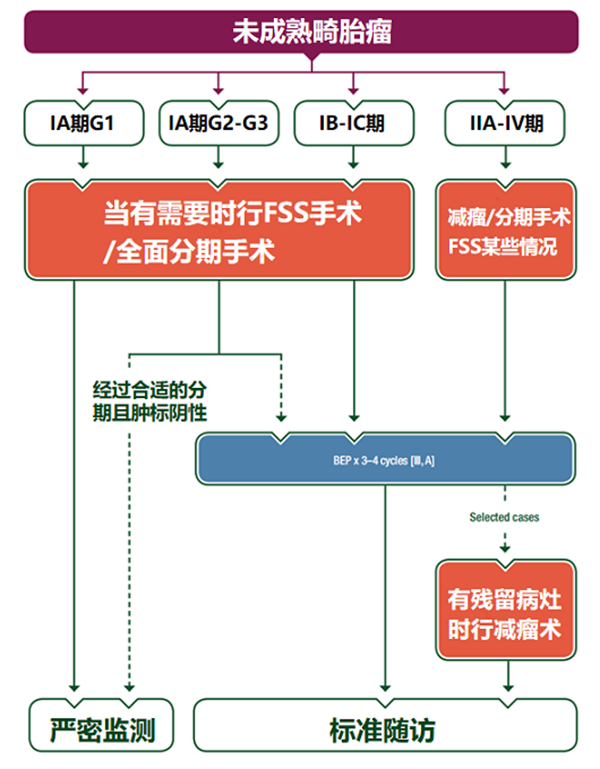
目前,BEP联合化疗(博来霉素、依托泊苷和顺铂)方案已被公认为MOGCT患者的标准辅助化疗方案。除了已知博来霉素引起不可逆的肺纤维化、顺铂导致骨髓抑制的风险外,依托泊苷还与致命的继发性急性髓系白血病/骨髓增生异常综合征有关。值得关注的是,BEP相关毒性中,由卵泡破坏、卵巢间质纤维化和原始卵泡减少导致的生育能力损害也是医生面临的一大挑战。
鉴于上述化疗药物的不良反应风险,特别是对年轻患者,因而有一些学者质疑对所有I期疾病患者辅助治疗的必要性。一些已发表的数据表明,所有分级的未成熟畸胎瘤和所有I期无性细胞瘤患者在行保留生育能力的手术之后,可以密切监测。由于复发后行辅助化疗的挽救率超过90%,有学者认为化疗可以留给术后证实复发的患者。然而,这种策略目前尚缺乏高质量循证医学证据的支持,安全性有待考证,也并没有被广泛接受[14]。
除此之外,生育咨询应成为MOGCT女性临床管理的重要组成部分。MOGCT女性要采用的第一种生育能力保护策略就是FSS。术后应充分评估患者的生育能力,在治疗结束后6个月常规评估卵巢功能,如检测抗缪勒氏管激素(AMH),其目的是及时判断生殖功能的损害程度、指导保留生育能力的选择。
如何在化疗期间更好地保护患者的卵巢功能也是医生面临的一大难题,GnRH-a的使用目前也尚缺乏高级别证据的支持。此外,卵母细胞冷冻保存或卵巢组织超低温保存等生育能力保存技术,也可以在必要时选择,这需要与生殖专家紧密合作。需要注意的是,对于术后不需要辅助化疗、仅监测即可的患者,除了随访原发疾病外,还必须对这些患者进行生殖内分泌评估。
四、小结
综上所述,鉴于MOGCT患者特殊的临床和病理特征,保留生育功能对这些患者来说具备可行性和必要性,手术范围趋向越来越保守(如不常规行大网膜和淋巴结切除),化疗期间如何更好地保护卵巢功能,如何与生殖专家更好地共同决策治疗方案等这些问题,均值得进一步的研究探索和临床实践。
参考文献
[1] Kumar S, Shah JP, Bryant CS, Imudia AN, Cote ML, Ali-Fehmi R, Malone JM Jr, Morris RT. The prevalence and prognostic impact of lymph node metastasis in malignant germ cell tumors of the ovary. Gynecol Oncol. 2008 Aug; 110(2): 125-32. doi: 10.1016/j.ygyno.2008.04.022. Epub 2008 Jun 20. PMID: 18571705.
[2] Guo H, Chen H, Wang W, Chen L. Clinicopathological Features, Prognostic Factors, Survival Trends, and Treatment of Malignant Ovarian Germ Cell Tumors: A SEER Database Analysis. Oncol Res Treat. 2021;44(4): 145-153.
[3] Gershenson DM. Management of ovarian germ cell tumors. J Clin Oncol 2007;25: 2938-43.
[4] Kurman, R.J.; Norris, H.J. Malignant Germ Cell Tumors of the Ovary. Hum. Pathol. 1977, 8, 551-564.
[5] Ertas, I.E.; Taskin, S.; Goklu, R.; Bilgin, M.; Goc, G.; Yildirim, Y.; Ortac, F. Long-term oncological and reproductive outcomes of fertility-sparing cytoreductive surgery in females aged 25 years and younger with malignant ovarian germ cell tumors. J. Obstet. Gynaecol. Res. 2014, 40, 797-805.
[6] Tamauchi, S.; Kajiyama, H.; Yoshihara, M.; Ikeda, Y.; Yoshikawa, N.; Nishino, K.; Utsumi, F.; Niimi, K.; Suzuki, S.; Kikkawa, F. Reproductive outcomes of 105 malignant ovarian germ cell tumor survivors:A multicenter study. Am. J. Obstet. Gynecol. 2018, 219, 385.
[7] Nasioudis D, Mastroyannis SA, Latif NA, Ko EM. Trends in the surgical management of malignant ovarian germcell tumors. Gynecol Oncol. 2020 Apr;157(1): 89-93.
[8] W. Xu, Y. Li, Is omentectomy mandatory among early stage (I, II) malignant ovarian germ cell tumor patients? A retrospective study of 223 cases, Int. J. Gynecol. Cancer 27(7) (2017) 1373-1378 Sep.
[9] Morice P, Denschlag D, Rodolakis A, Reed N, Schneider A, Kesic V, et al.Recommendations of the Fertility Task Force of the European Society of Gynecologic Oncology about the conservative management of ovarian malignant tumors. Int J Gynecol Cancer 2011; 21:951-63.
[10] Parkinson CA, Hatcher HM, Earl HM, Ajithkumar TV. Multidisciplinary management of malignant ovarian germ cell tumours. Gynecol Oncol 2011;121: 625-36.
[11] Chan JK, Tewari KS, Waller S, Cheung MK, Shin JY, Osann K, et al. The influence of conservative surgical practices for malignant ovarian germ cell tumors. J Surg Oncol 2008;98: 111-6.
[12] Weinstein D, Polishuk WZ. The role of wedge resection of the ovary as a cause for mechanical sterility. Surg Gynecol Obstet 1975;141:417-8.
[13] NCCN Guideline Version 1. 2022 Ovarian Cancer / Fallopian Tube Cancer / Primary Peritoneal Cancer.
[14] Ray-Coquard, I.; Morice, P.; Lorusso, D.; Prat, J.; Oaknin, A.; Pautier, P.; Colombo, N. Non-epithelial Ovarian Cancer: ESMO Clinical Practice Guidelines for Diagnosis, Treatment and Follow-up. Ann Oncol. 2018, 29 (Suppl. 4), iv1–iv18.
作者简介

王雅卓 主治医师
王雅卓,博士,主治医师,河北省人民医院妇科工作。社会职务:河北省妇幼保健协会妇女健康管理专业委员会委员、河北省疼痛医学会妇科专业委员会委员、河北省优生优育协会阴道镜和宫颈病理学专业委员会委员。专业特长:熟练掌握妇科常见病及多发病的诊治,擅长宫颈病变诊治和妇科良恶性肿瘤的治疗,主要从事妇科恶性肿瘤的基础与临床研究。科研成果及获奖情况:参与省级科研课题3项,发表论文及著作十余篇;获得“思辨卓行”辩论赛全国二等奖、河北医科大学英文授课竞赛二等奖、河北省人民医院科普大赛二等奖、河北省人民医院授课竞赛二等奖。
声明:本文为作者原创投稿并授权发布,文章仅代表作者观点,不代表本平台立场。如需转载请留言获取授权,未经授权谢绝转载。
投稿邮箱:fcktougao@126.com
 妇产科在线APP下载
妇产科在线APP下载













