美国妇科肿瘤学会(SGO)2022年会于3月18日至21日以线下结合线上会议的形式召开。作为全球妇科肿瘤领域的盛会,SGO年会汇聚了妇科肿瘤学领域的顶尖专家和学者,展示妇科肿瘤领域最新的研究进展及最佳的临床实践。

宫颈癌是女性生殖系统的常见恶性肿瘤,首都医科大学附属北京妇产医院吴玉梅教授团队全程关注SGO 2022年会上HPV感染和宫颈癌等方面的最新进展,精心筛选出会议上的重要发言和临床研究进展,形成系列报道,与广大读者分享。
撰稿:常虹博士、吉晨博士、王娇博士、王明博士、邢艳博士、张晶晶博士
审核:何玥教授、吴玉梅教授
单位:首都医科大学附属北京妇产医院
一、Wenfang Tian教授:10年多中心回顾性研究,分析低风险的IA1-IB1期宫颈癌患者接受腹腔镜下根治性手术的预后
背景:对于早期宫颈癌患者,越来越多的证据显示开腹根治性手术(OARH)比腹腔镜根治性手术(LRH)有更好的生存预后。然而,受限于IA及低风险IB期宫颈癌患者少,仍需更多的研究证实。本研究的目的是进一步评估LRH治疗低危型IA1-IB1期宫颈癌患者的生存预后。低危患者的定义是肿瘤最大径线≤2 cm、浸润宫颈间质深度<1/3、无淋巴结转移。
方法:回顾性收集了2010年1月至2020年12月在三家医院(湖南省肿瘤医院、邵阳市中心医院、岳阳市第一人民医院)接受腹腔镜或开腹根治性手术的IA1、IA2及IB1期(2018年FIGO分期)宫颈癌患者。对比OARH与LRH组的无进展生存期(PFS)及总生存期(OS)。
结果:筛选了2010年1月至2020年12月诊治的5360例患者,1850(35%)符合入组条件。其中1090例患者接受了开腹手术,760例患者接受了腹腔镜手术。在整个队列中,两组患者的临床特点相似,如年龄、BMI、FIGO分期、病理类型和分化、盆腔淋巴结、切缘阳性、宫颈间质浸润深度、淋巴脉管间隙受侵及辅助治疗。对比LRH和OARH,LRH组在失血量、输血率及住院时间方面更有优势。亚组分析中,对于低危组患者(肿瘤≤2 cm,宫颈浅层间质浸润、无脉管间隙受侵、无淋巴结转移),LRH组的DFS及OS与OARH组相当。但当肿瘤>2 cm或合并其他中危和高危因素时,LRH组的PFS及OS更短,这与LACC试验结果一致。
结论:对低危IA1-IB1期宫颈癌患者,腹腔镜和开腹手术对生存无影响。仍需更多的前瞻性研究探索IA1-IB1期低危宫颈癌患者的预后。对于有高危因素的患者,腹腔镜手术比开腹手术的肿瘤预后更差。

二、M. Rush教授:新辅助化疗联合根治性手术治疗局部晚期宫颈癌患者的预后
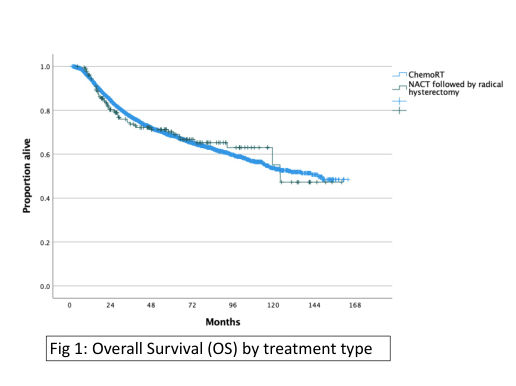
背景:以铂类为基础的化疗联合放疗是局部晚期宫颈癌患者的标准治疗方案。然而,对于IB2-II期患者,新辅助化疗(NACT)联合根治性手术已被认为是另一种治疗策略。本研究旨在分析NACT联合根治性手术治疗局部晚期宫颈癌患者的可行性及预后。
方法:利用国家癌症数据网络纳入患者,即病理诊断为宫颈鳞癌、腺癌及腺鳞癌,FIGO分期为IB2-II期;2004-2015年间确诊;放化疗组(盆腔外照射至少45 Gy,同步增敏化疗);NACT/手术组(根治性手术前接受化疗1~6个周期)。
结果:182例患者接受了NACT联合根治性手术,3859例患者接受同步放化疗。NACT联合手术组患者切缘阳性率为7%,中位住院3天,再次入院率为5.1%,90.1%患者术后接受了辅助放疗,46.7%的患者接受了近距离照射。对比施行同步放化疗的患者,接受NACT联合根治性手术的患者更年轻,更多分期为IB2期以及病理为腺癌的患者。IB2期患者的OS与II期患者无差异。在校正了年龄、种族、合并症、病理类型和分期等因素后,NACT联合根治性手术组并不延长OS(HR=1.05,95%CI 0.80~1.38)。
结论:采用NACT联合根治性手术治疗与同步放化疗患者的OS相当,没有生存优势及潜在增加死亡率,在医疗资源丰富的地区,初始同步放化疗仍应该是更为推荐的治疗方式。
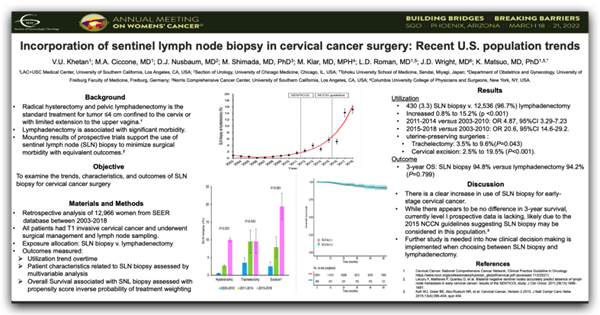
三、U. V. Khetan教授:前哨淋巴结活检在美国宫颈癌患者⼿术中的应⽤
背景:根治性⼦宫切除术和盆腔淋巴结切除术是局限于宫颈或局限于阴道上部的≤4 cm宫颈癌患者的标准治疗⽅法。腹膜后淋巴结切除与发病显著相关。越来越多的前瞻性试验结果⽀持使⽤前哨淋巴结(SLN)活检,以同等效果将⼿术发病率降⾄最低。
目的:探讨宫颈癌患者手术中SLN活检的应用趋势、特点和结果。
材料与方法:回顾性分析了2003至2018年来⾃SEER数据库中的12966例⼥性。所有患者均为T1浸润性宫颈癌,并接受了⼿术治疗和淋巴结取样。分组依据SLN活检与淋巴结切除术。使⽤趋势超时分析结果。通过多因素分析评估与SLN活检相关的患者特征。与SNL活检相关的总⽣存率通过倾向评分和治疗加权的反概率进⾏评估。
结果:430例(3.3%)⾏SLN活检,12536例(96.7%)⾏淋巴结切除,增加0.8%~15.2%(P<0.001)。2011-2014 vs. 2003-2010,OR=4.87,95%CI 3.29~7.23;2015-2018 vs. 2003-2010,OR=20.6,95%CI 14.6~29.2.。保留⼦宫的⼿术:根治性宫颈切除术,3.5%~9.6%(P=0.043);部分宫颈切除:2.5%~19.5%(P<0.001)。SLN活检组3年OS为94.8%,淋巴结切除组为94.2%(P=0.799)。
讨论:SLN活检在早期宫颈癌患者中的应⽤明显增加。虽然3年⽣存率似乎没有差异,但⽬前缺乏I级前瞻性数据,可能是因为2015年NCCN指南建议在该⼈群中考虑SLN活检。在选择SLN活检和淋巴结切除术时如何进⾏临床决策,还需要进⼀步研究。
四、Steven B Holloway教授:帕博利珠单抗治疗晚期、转移性宫颈/外阴/阴道癌患者的真实世界经验
背景:复发性宫颈癌是⼀种难以治疗的疾病,总体预后较差。根据II期KEYNOTE-158研究的初步结果,帕博利珠单抗于2018年6⽉获得FDA加速批准,⽤于治疗预处理复发性或转移性宫颈癌患者。虽然临床试验报告的缓解率仅有12%,但许多患者表现出持久的缓解,⼀些患者的治疗持续时间超过12个⽉。鉴于这些有利的结果,本研究在学术和安全⽹医院系统中分析这种治疗⽅案的实际纳⼊和使⽤情况,并评估患者结果。
材料与方法:基于FDA加速批准帕博利珠单抗的时机,并允许引⼊时间,机构数据审查确定了预处理的复发性、持续性或转移性宫颈、阴道或外阴癌女性,计划从2017⾄2021年接受帕博利珠单抗治疗。从病历中收集⼈⼝统计学和临床病理学数据,分析治疗持续时间、治疗相关不良事件和临床结果。排除标准包括⼦宫或卵巢原发性肿瘤、PD-L1阴性状态以及最终未接受第⼀周期治疗的患者。
结果:52例患者确定接受帕博利珠单抗治疗。在考虑排除标准后,20例患者被纳⼊分析。未开始使⽤帕博利珠单抗治疗的最常见原因是失访、PD-L1阴性肿瘤或纳⼊其他临床试验。患者中位年龄56岁,其中宫颈癌最常⻅(占80%),其余有复发性外阴癌(占15%)或阴道癌(占5%)。之前接受系统性治疗的中位数为1(最多为4)。客观有效率为11.7%,临床受益率(包括病情稳定)为47%。总体治疗中位持续时间(mDOT)为2.1个⽉(2个周期,IQR 1~8)。在疾病进展或死亡的患者中,mDOT为2.1个⽉(2个周期,IQR 2~3)。然⽽,该组25%的患者⾄少接受了10个周期的治疗,所有患者⽬前仍在接受治疗(mDOT:13个⽉)。治疗耐受性良好,25%的受试者出现任何级别的毒性,其中⼤多数为2级甲减,仅通过药物治疗即可。1名患者出现了严重毒性,即3级免疫介导的结肠炎,最终导致其在1个周期后停药。
结论:与已发表的临床试验结果相⽐,帕博利珠单抗用于复发性宫颈癌、阴道癌、外阴癌患者真实世界治疗中的耐受性良好。1/4的患者经历了毒性最⼩的持久反应,并持续治疗超过1年。

五、D. Nasioudis教授:盆腔廓清术治疗IVA期宫颈癌患者的预后
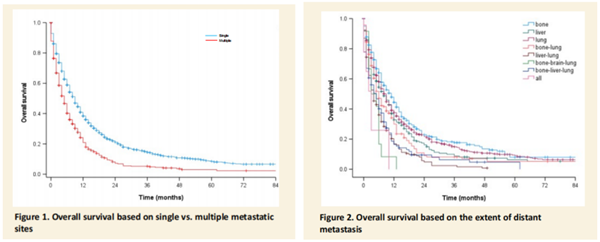
美国Sarah Joh教授团队开展了一项回顾性队列研究,利用SEER数据库中2010至2018年间的数据,分析了IV期宫颈癌患者不同转移部位对预后的影响。
研究纳入1772例IVB期宫颈癌患者,肿瘤转移部位包括骨、脑、肝或肺。评估变量因素包括患者(年龄、种族/民族和登记区域)、肿瘤特征(组织学亚型、肿瘤分化、T和N分类),以及治疗(化疗)。在多变量分析中,根据解剖部位和远处器官转移程度评估患者总生存期。
结果显示,IVB期患者最常见的转移部位为肺(1210例,占68.3%),其次为骨(623例,占35.2%)、肝(531例,占30.0%)、脑(21例,占1.2%)。470例(26.5%)患者发生多器官转移,肝/肺转移是最常见的转移模式(170例,占9.6%),其次是骨/肺(166例,占9.4%),再次是骨/肝(113例,占6.4%)。在多变量分析中,与单器官转移相比,多器官转移者的死亡风险增加50%(HR=1.50,95%CI 1.33~1.69)。IVB期宫颈癌患者的生存结果因转移部位和数量的不同而有很大差异。将单个和多个远端器官转移(IVB1和IVB2)加入癌症分期中,这种分层分期可指导临床医生做出治疗计划选择。
专家简介

吴玉梅教授
主任医生、二级教授、博士生导师,首都医科大学附属北京妇产医院妇瘤科主任。
学术兼职:中华医学会妇科肿瘤分会委员、北京医学会妇科肿瘤学分会副主任委员、北京妇产学会外阴阴道疾病分会副主委、北京医学会肿瘤学分会委员、中国老年医学学会妇科分会会长。
擅长领域:致力于妇科肿瘤临床、科研和教学工作。
主要研究方向:宫颈癌放射敏感及放射抵抗机制、妊娠合并宫颈病变的筛查策略、妇科恶性肿瘤的预防。
科研成果:发表妇科肿瘤相关SCI论文30余篇,中文核心期刊论文100余篇;主持国家基金、省科技重点研发项目等多项,获省部级科技奖3项,国家发明专利1项。
个人荣誉:全国医德标兵、北京市先进工作者、北京市三八红旗奖章等。

何玥教授
医学博士,首都医科大学附属北京妇产医院妇瘤科副主任医师,在各类妇科肿瘤领域尤其是宫颈癌综合治疗方面有较丰富的临床经验并有深入的研究,曾于德国进修妇产科学;兼任北京医学会妇科肿瘤学分会青年委员、中国老年医学学会妇科分会青年委员、北京医学会外阴阴道疾病学会秘书。
第一作者发表SCI文章9篇,累计IF达20分,发表核心期刊文章10余篇,参与编写翻译书籍3部。近5年主持国自然、北京市教委、首都卫生发展专项、北京市医管局“青苗计划”、北京市优秀人才等科研课题。
吴玉梅教授硕博士报道团队

常虹博士、吉晨博士、王娇博士

王明博士、邢艳博士、张晶晶博士
 妇产科在线APP下载
妇产科在线APP下载













